牛血清白蛋白(Bovine serum albumin,BSA)是胎牛血清中的主要成分,广泛应用在抗体药物、疫苗药物以及CGT药物等生物制品的生产过程中。对于疫苗类药物,目前很多病毒性疫苗产品(如狂犬、麻疹、腮腺炎、风疹、水痘疫苗等)是采用细胞培养法生产的,因此牛血清白蛋白(BSA)残留量的检测是疫苗产品中重要的质控指标,直接关系到疫苗使用的安全性。

君研BSA检测
君研生物自主研发生产的BSA定量检测试剂盒(酶联免疫吸附法),具有灵敏度高、稳定性好、特异性强等优势,并经过了全面的性能验证。该试剂盒中标准品已溯源至国家标准品,并遵循ISO13485质量管理体系进行研发生产。
产品优势 | PRODECT ADVANTAGE

性能指标 | PERFORMANCE INDEX

标准曲线验证:
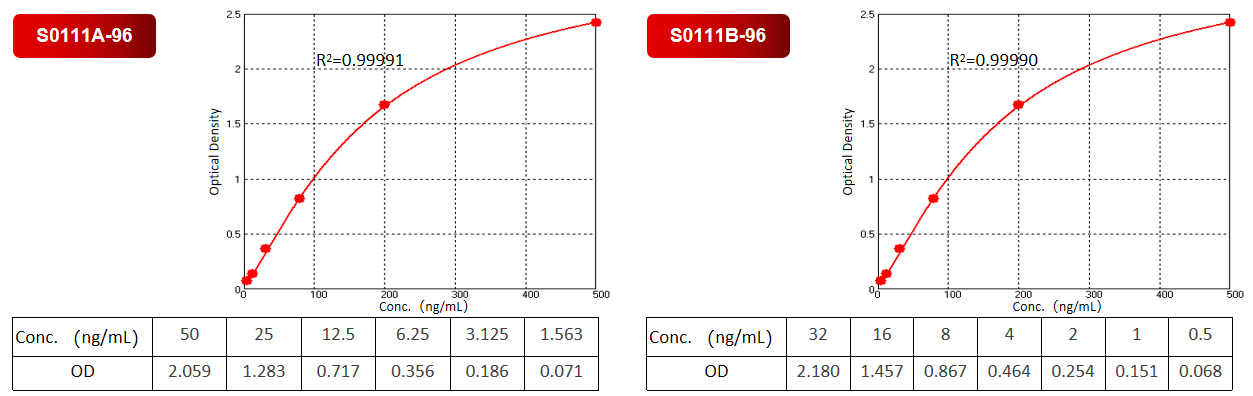
标准曲线是经4-PL拟合得到,S0111A-96检测范围在1.56-50ng/mL,S0111B-96检测范围在0.5-32ng/mL,R2均可达到0.99。
试剂盒准确度:
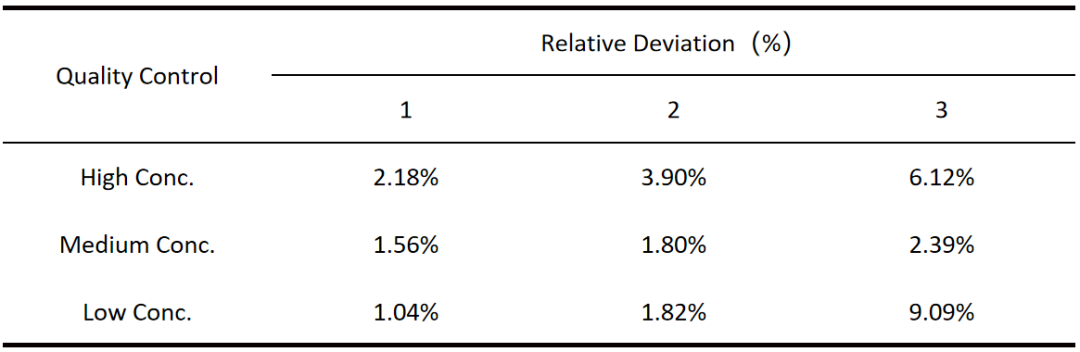
经验证,君研生物BSA定量检测试剂盒(S0111A-96)高、中、低浓度质控品测量偏差均≤15%。
试剂盒精密度:
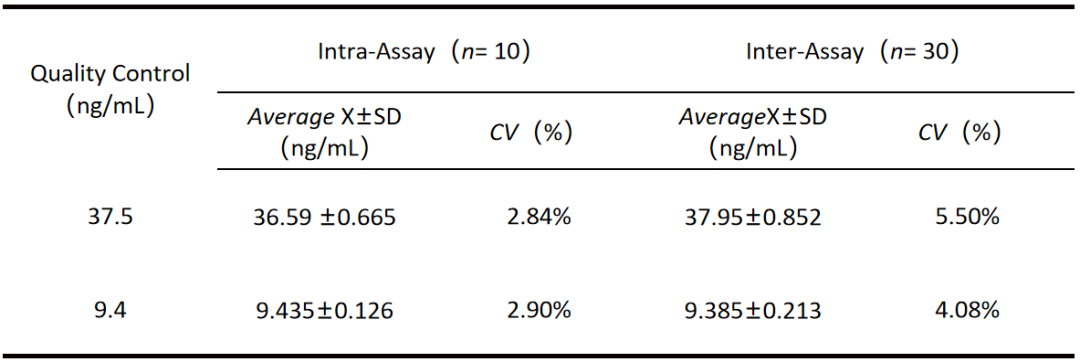
经验证,君研生物BSA定量检测试剂盒(S0111A-96)批内差≤10%,批间差≤15%,精密度符合标准。
样品加标回收率检测:
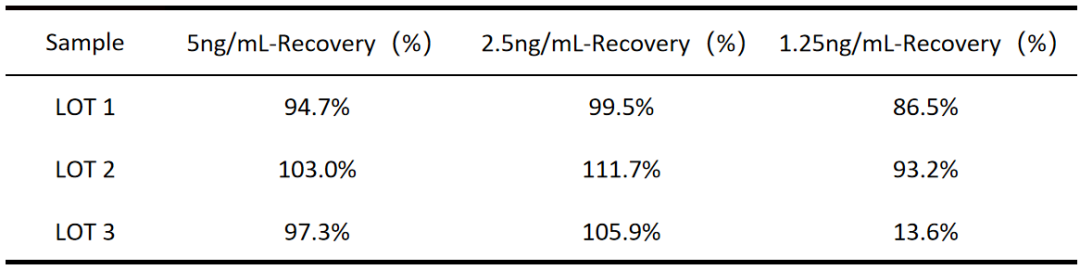
经验证,君研生物BSA定量检测试剂盒(S0111A-96)实际样品高、中、低浓度加标回收率均在70%~130%范围内。
君研产品推荐
JUNYAN PRODUCTS

地址:山西省太原市小店区唐槐路与晋善街交叉口东北角第1号地2期13号楼
区域经理:18701864343/13701962646(上海)
15851483166(江苏、浙江)
15234188795(全国)
技术支持:18536588361、19503412257
邮箱:sales@junyanbios.cn 订购咨询
mkt@junyanbios.cn 商务合作